مقدمه
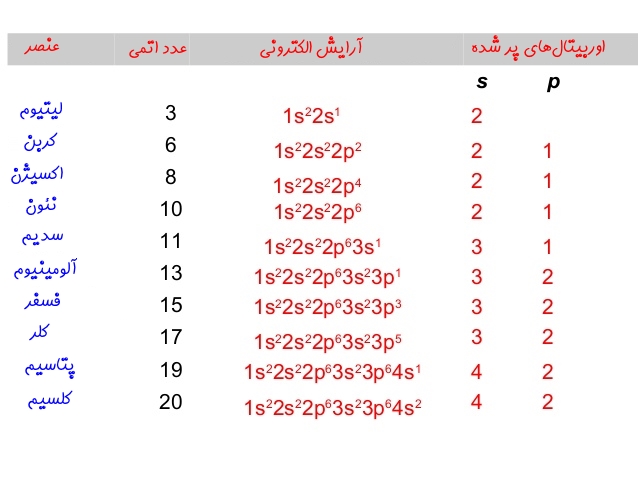
به کمک مدل کوانتومی اتم میتوانیم چگونگی آرایش الکترونها در اتم را تعیین کنیم. الکترونها همواره تمایل دارند تا در پایینترین تراز انرژی قرار گیرند یا اوربیتالی را زودتر پر کنند که سطح انرژی آن پایینتر است (طرح آفبا). از آنجا که یادگیری و حفظ ترتیب پر شدن زیرلایهها برای دانشآموزان چالش بزرگی است در این مقاله، یادگیری ترتیب پر شدن زیرلایهها به روشی بسیار ساده، جذاب، کاربردی و در مدتزمان کوتاه و همچنین رسم آرایش الکترونی اتمهایی با عدد اتمی کوچک و بزرگ مورد بررسی قرار میگیرد. روش اجرا
پس از اینکه دانشآموزان با مفاهیم عددهای کوانتومی و توزیع الکترونها در لایهها و زیرلایهها آشنا شدند، این روش اجرا میشود. نخست مانند آنچه در شکل۱ دیده میشود مثلثی شامل خطوط افقی برای نمایش 7….1،2=n رسم میکنیم. عددهای ۱ تا ۷ را از رأس مثلث در دو سمت چپ و راست قرار میدهیم. میبینید که با گذاشتن s، در کنار عددهای سمت چپ، کار با نخستین عدد کوانتومی روی شکل تمام شده است. اکنون در کنار عددهای سمت راست مثلث، حرف p را به عنوان دومین عدد کوانتومی فرعی قرار میدهیم. برای عدد کوانتومی بعدی یعنی d و اوربیتال f، از داخل مثلث استفاده میکنیم. با توجه به جدول تناوبی، اوربیتال 3d در عنصرهای تناوب چهارم در حال پرشدن است. پس روی خط مربوط به تناوب چهارم تا هفتم، اوربیتالهای d را قرار میدهیم و آنها را به ترتیب، با شماره 3 تا 6 مشخص میکنیم. حالا نوبت به اوربیتال 4f میرسد. با توجه به جدول در تناوب ششم، اوربیتال 4f شروع به پرشدن میکند. پس روی دو خط مربوط به تناوب شش و هفت، این اوربیتال را مشخص میکنیم و به ترتیب، شمارههای ۴ و ۵ را در کنار آنها میگذاریم. اگر این مثلث را در ذهن داشته باشیم به راحتی میتوانیم آرایش الکترونی اتمهای مختلف را با شروع از رأس مثلث و به ترتیب، پر کردن زیرلایهها از خطی به خط دیگر، در کوتاهترین زمان رسم کنیم.
آرایش الکترونی اتمها را به شیوه دیگری نیز میتوان نوشت که آرایش الکترونی فشرده نام دارد. در این آرایش الکترونی نماد شیمیایی گاز نجیب پیش از اتم مورد نظر را داخل کروشه قرار میدهیم، سپس با استفاده از شکل ۱، شروع به پر کردن زیرلایهها میکنیم.
16S :[Ne] 3s3 2p4
35Br :[Ar] 3d4 10s4 2p5
72Hf :[Xe] 4f5 14d6 2s2
چگونه آرایش الکترونی بنویسیم
توجه
در این روش برای رسم آرایش الکترونی هافنیم با توجه به شکل مثلث، پس از نوشتن گاز نجیب زنون ـ که در دوره پنجم قرار دارد ـ عدد زیرلایهها را از کوچک به بزرگ مینویسیم (۴ و ۵ و ۶) اما برای پر کردن الکترون در زیرلایهها با توجه به شکل مثلث، ترتیب قرار گرفتن زیرلایهها را رعایت میکنیم. یعنی در آغاز ۲ الکترون در 6s، سپس ۱۴ الکترون در 4f، و در انتها ۲ الکترون در 5d قرار میدهیم.
آرایش الکترونی شرایط خاص
قاعده آفبا، آرایش الکترونی اغلب عنصرها را به خوبی پیشبینی میکند ولی برای برخی عنصرهای جدول، نارسایی دارد. روشهای پیچیده طیفسنجی که آرایش الکترونی اتمها را با دقت تعیین میکند، نشان میدهد که اتمهای کروم و مس هریک در بیرونیترین زیرلایه خود فقط یک الکترون دارند.
24Cr :[Ar] 3d4 5s1
24Cr :[Ar] 3d4 4s2
29Cu :[Ar] 3d4 10s1
29Cu :[Ar] 3d4 9s2
بررسیهای دقیق طیفسنجی نشان میدهد که دو عنصر نقره و مولیبدن هم هر یک در بیرونیترین زیرلایه خود فقط یک الکترون دارند.
42Mo :[Kr] 4d5 5s1
42Mo :[Kr] 4d5 4s2
47Ag :[kr] 4d5 10s1
47Ag :[kr] 4d5 9s2
نتیجهگیری
در این تجربه آموزشی با استفاده از یک شکل بسیار ساده:
ـ یادگیری ترتیب پرشدن زیرلایهها به روش بسیار ساده و نوین آموزش داده شد.
ـ رسم آرایش الکترونی اتمها، بهویژه اتمهایی که دارای عدد اتمی بزرگ هستند و حفظ ترتیب پرشدن آنها که چالشی و طاقتفرسا بود، به صورت آسان و کاربردی بیان شد.
ـ رسم آرایش الکترونی اتمها بهصورت فشرده توضیح داده شد.
ـ آرایش الکترونی اتمها در شرایط خاص بیان شد.
ـ دانشآموزان در کمترین زمان ممکن توانستند آرایش الکترونی اتمها را رسم کنند.
ـ این روش نه تنها برای دانشآموزان پایه دهم، بلکه برای دانشآموزان کنکوری سودمند و کاربردی است.
این نتایج با توجه به پاسخ درست دانشآموزان به پرسشهای مفهومی و متنوع هنگام تدریس، پرسش آزمونهای پایانی و کنکور بهدست آمد و نشان داد که دانشآموزان به درک بهتری از مفاهیم مربوط به رسم آرایش الکترونی در مدت زمان کوتاه دستیافتهاند.
12.13 from (96-97) MATN SHIMI 121-min-3_19971.pdf![]()
آرایش الکترونی (به انگلیسی: Electron configuration) نحوه چینش الکترونها در اوربیتالها اطراف هسته اتم را نشان میدهد؛ و شیوه پر شدن زیر لایهها به ترتیب زیر است:
1s 2s 2p 3s 3p 4s 3d 4p 5s 4d 5p 6s 4f 5d 6p 7s 5f 6d 7p
در s حداکثر ۲ الکترون در p حداکثر ۶ الکترون در d حداکثر ۱۰ و در f حداکثر ۱۴ الکترون قرار میگیرد. به طور مثال آرایش الکترونی گالیوم که ۳۱ الکترون دارد به صورت زیر نوشته میشود:
۱s۲۲s۲۲p۶۳s۲۳p۶۴s۲۳d۱۰۴p۱
که البته به صورت مرتب شده و به شکل زیر نوشته میشود
چگونه آرایش الکترونی بنویسیم
۱s۲۲s۲۲p۶۳s۲۳p۶۳d۱۰۴s۲۴p۱
نکته مهم : در آرایش الکترونی اتم خنثی هرگز زیرلایه d4 یا d9 نداریم دراین حالت باید از زیر لایه s کناری 1 الکترون کم کرده وبه زیر لایه dمیدهیم بر فرض مثال ارایش الکتروونی عنصر مس 29 بدینگونه می باشد:
1s2 2s2 2p6 3s2 3p6 3d9 4s2 براساس نکته بالا ما باید از زیر لایه sیک الکترون به d بدهیم و تمام که میشود:
1s2 2s2 2p6 3s2 3p6 3d10 4s1.
اصل آفبا (به آلمانی: Aufbau)، به معنی ساختن یکی از اصول آرایش الکترونی است که میگوید:
ترتیب عناصر پرشدن لایه ی الکترونی ب صورت ۲(۸(۸(۲(است و اگر الکترون باقی ماند آنرا ب لایه ی سوم یعنی:۲(۸+۸(۸(۲(پر میکنیم.(لایه ی سوم را تا سقف ۱۸الکترون میتوان پر کرد)
این اصل برای ۱۸ عنصر اول به خوبی صدق میکند. اما اصل مادلونگ که در سال ۱۹۳۶ و توسط آروین مادلونگ ارائه شد به خوبی تا ۱۰۰ عنصر اول صدق میکند[۱]
از طریق این اصل ترتیب پرشدن اوربیتالها بدین گونه است:
آرایش الکترونی (به انگلیسی: Electron configuration) نحوه چینش الکترونها در اوربیتالها اطراف هسته اتم را نشان میدهد؛ و شیوه پر شدن زیر لایهها به ترتیب زیر است:
1s 2s 2p 3s 3p 4s 3d 4p 5s 4d 5p 6s 4f 5d 6p 7s 5f 6d 7p
در s حداکثر ۲ الکترون در p حداکثر ۶ الکترون در d حداکثر ۱۰ و در f حداکثر ۱۴ الکترون قرار میگیرد. به طور مثال آرایش الکترونی گالیوم که ۳۱ الکترون دارد به صورت زیر نوشته میشود:
۱s۲۲s۲۲p۶۳s۲۳p۶۴s۲۳d۱۰۴p۱
که البته به صورت مرتب شده و به شکل زیر نوشته میشود
چگونه آرایش الکترونی بنویسیم
۱s۲۲s۲۲p۶۳s۲۳p۶۳d۱۰۴s۲۴p۱
نکته مهم : در آرایش الکترونی اتم خنثی هرگز زیرلایه d4 یا d9 نداریم دراین حالت باید از زیر لایه s کناری 1 الکترون کم کرده وبه زیر لایه dمیدهیم بر فرض مثال ارایش الکتروونی عنصر مس 29 بدینگونه می باشد:
1s2 2s2 2p6 3s2 3p6 3d9 4s2 براساس نکته بالا ما باید از زیر لایه sیک الکترون به d بدهیم و تمام که میشود:
1s2 2s2 2p6 3s2 3p6 3d10 4s1.
اصل آفبا (به آلمانی: Aufbau)، به معنی ساختن یکی از اصول آرایش الکترونی است که میگوید:
ترتیب عناصر پرشدن لایه ی الکترونی ب صورت ۲(۸(۸(۲(است و اگر الکترون باقی ماند آنرا ب لایه ی سوم یعنی:۲(۸+۸(۸(۲(پر میکنیم.(لایه ی سوم را تا سقف ۱۸الکترون میتوان پر کرد)
این اصل برای ۱۸ عنصر اول به خوبی صدق میکند. اما اصل مادلونگ که در سال ۱۹۳۶ و توسط آروین مادلونگ ارائه شد به خوبی تا ۱۰۰ عنصر اول صدق میکند[۱]
از طریق این اصل ترتیب پرشدن اوربیتالها بدین گونه است:
آرایش الکترونی (به انگلیسی: Electron configuration) نحوه چینش الکترونها در اوربیتالها اطراف هسته اتم را نشان میدهد؛ و شیوه پر شدن زیر لایهها به ترتیب زیر است:
1s 2s 2p 3s 3p 4s 3d 4p 5s 4d 5p 6s 4f 5d 6p 7s 5f 6d 7p
در s حداکثر ۲ الکترون در p حداکثر ۶ الکترون در d حداکثر ۱۰ و در f حداکثر ۱۴ الکترون قرار میگیرد. به طور مثال آرایش الکترونی گالیوم که ۳۱ الکترون دارد به صورت زیر نوشته میشود:
۱s۲۲s۲۲p۶۳s۲۳p۶۴s۲۳d۱۰۴p۱
که البته به صورت مرتب شده و به شکل زیر نوشته میشود
چگونه آرایش الکترونی بنویسیم
۱s۲۲s۲۲p۶۳s۲۳p۶۳d۱۰۴s۲۴p۱
نکته مهم : در آرایش الکترونی اتم خنثی هرگز زیرلایه d4 یا d9 نداریم دراین حالت باید از زیر لایه s کناری 1 الکترون کم کرده وبه زیر لایه dمیدهیم بر فرض مثال ارایش الکتروونی عنصر مس 29 بدینگونه می باشد:
1s2 2s2 2p6 3s2 3p6 3d9 4s2 براساس نکته بالا ما باید از زیر لایه sیک الکترون به d بدهیم و تمام که میشود:
1s2 2s2 2p6 3s2 3p6 3d10 4s1.
اصل آفبا (به آلمانی: Aufbau)، به معنی ساختن یکی از اصول آرایش الکترونی است که میگوید:
ترتیب عناصر پرشدن لایه ی الکترونی ب صورت ۲(۸(۸(۲(است و اگر الکترون باقی ماند آنرا ب لایه ی سوم یعنی:۲(۸+۸(۸(۲(پر میکنیم.(لایه ی سوم را تا سقف ۱۸الکترون میتوان پر کرد)
این اصل برای ۱۸ عنصر اول به خوبی صدق میکند. اما اصل مادلونگ که در سال ۱۹۳۶ و توسط آروین مادلونگ ارائه شد به خوبی تا ۱۰۰ عنصر اول صدق میکند[۱]
از طریق این اصل ترتیب پرشدن اوربیتالها بدین گونه است:
همانطور که میدانید نوشتن آرایش الکترونی فشرده برای کنکور و شیمی دبیرستان بسیار لازم و ضروری است. روش معمول برای نوشتن آرایش الکترونی فشرده بسیار وقتگیر و پیچیده است.
در این مطلب قصد دارم یک روش ساده و سریع برای نوشتن آرایش الکترونی فشرده عناصر به شما آموزش بدهم.
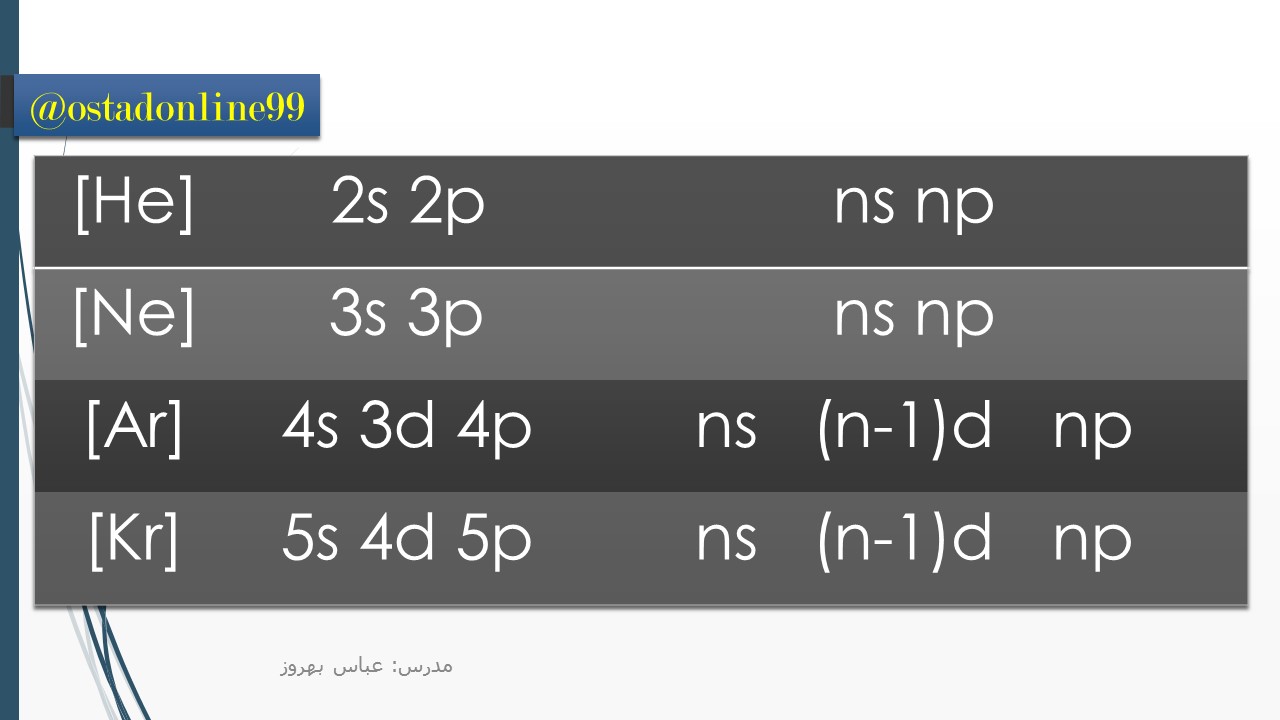
اگر گروه عناصر گازهای نجیب را به ترتیب و همراه با عدد اتمی و شماره تناوب آنها را به خوبی حفظ کرده باشید با استفاده از جدول بالا به راحتی قادر به نوشتن آرایش الکترونی فشرده خواهید بود.
اگر عدد اتمی یک عنصر را داشته باشیم، گاز نجیب ماقبل آنرا شناسایی کرده و بعد طبق جدول آرایش الکترونی را مینویسیم. سپس عدد اتمی آنرا منهای عدد اتمی گاز نجیب کرده تعداد الکترونهای بدست آمده را به ترتیب در زیرلایه های بدست آمده پر میکنیم.
چگونه آرایش الکترونی بنویسیم
به عنوان مثال اگر عدد اتمی عنصری 31 باشد در تناوب چهارم قرار دارد و گاز نجیب ماقبل آن آرگون است. در جدول ردیف آرگون را پیدا کرده و زیرلایه ها را مینویسیم:
[Ar] 4s 3d 4p
31-18=13
[Ar] 4s2 3d10 4p1
[Ar] 3d10 4s2 4p1
پیشتر در وبلاگ فرادرس مدل اتمی بور را توضیح دادیم. مدل اتمی بور مدلی یکبعدی است که تنها از یک عدد جهت توصیف الکترونهای یک اتم استفاده میکند. این عدد همان n است که نشان دهنده لایهای است که الکترون در آن میچرخد. همچنین مدل مذکور تنها میتواند ویژگیهای اتم هیدروژن را توجیه کند.
محتوای این مطلب جهت یادگیری بهتر و سریعتر آن، در انتهای متن به صورت ویدیویی نیز ارائه شده است.
«اروین شرودینگر» (Erwin Schrödinger)، در سال ۱۹۲۶ با استفاده از محاسبات پیچیده ریاضی نشان داد که الکترونهای یک اتم در مسیرهایی سهبعدی حرکت میکنند؛ از این رو به سه عدد جهت توصیف الکترونها نیازمندیم. البته به عدد چهارمی نیز بهمنظور نشان دادن نحوه حرکت الکترون به دور خودش نیازمند هستیم. هر الکترون در فضایی ابری تحت عنوان اوربیتال در حال حرکت است. نحوه این حرکت و آرایش الکترونها در شکلگیری پیوندهای شیمیایی بسیار تاثیرگذار هستند. با استفاده از اعداد کوانتومی که در ادامه به آنها خواهیم پرداخت، میتوان اوربیتالها را به شکلی دقیقتر توصیف کرد.
شرودینگر با حل معادلاتش سه عدد را جهت توصیف الکترونهای یک اتم ارائه داد. این اعداد عبارتند از:
عدد کوانتومی اصلی یا n، نشان دهنده اندازه و انرژی اوربیتال است. منظور از اندازه اوربیتال، فاصله الکترونها از هسته اتم است. هرچه اندازه این عدد بیشتر باشد، اندازه و انرژی اوربیتال نیز بزرگتر خواهد بود. تمامی الکترونهایی که n آنها با هم برابر است، در فاصلهای یکسان از هسته اتم قرار میگیرند.
چگونه آرایش الکترونی بنویسیم
L یا عدد کوانتومی فرعی، نشاندهنده شکل اوربیتال است. یک لایه با عدد کوانتومی n میتواند از n-1 اوربیتال مختلف تشکیل شده باشد. شکلهای یک اوربیتال را با نمادهای $$s,p,d,f,…$$ نشان میدهند. برای نمونه L=۰ نشان دهنده اوربیتال s یا L=۱ اوربیتال p را نشان میدهد. تصویر ارائه شده، شکل اوربیتالهای مختلف را نمایش میدهد.
با توجه به شکل فوق، اوربیتال s کروی بوده و تنها به یک صورت میتواند در فضا قرار گیرد. اما مثلا اوربیتال p میتواند هم در راستای محور z و هم در راستای محور x جهتگیری کند. از این رو به عدد سومی تحت عنوان m یا عدد کوانتومی مغناطیسی نیازمندیم تا این جهتگیری اوربیتالها را نشان دهیم. بنابراین عدد m جهتگیری اوربیتال را در فضا نشان میدهد. عدد کوانتومی مغناطیسیِ یک اوربیتال، بین L- و L+ قرار دارد. برای نمونه اعداد کوانتومی مغناطیسی برای اوربیتال p که L مربوط با آن ۱ است، برابر با 1+,1,0- در نظر گرفته میشوند.
اگر الکترون را به صورت یک کره در نظر بگیریم، با استفاده از ۳ عدد معرفی شده در بالا میتواند جهت حرکت آن را در فضا مشخص کرد. اما این الکترون، به دور خودش نیز در حال چرخش است. این چرخش را با عدد کوانتومی اسپینی یا ms نشان میدهند. بنابراین یک الکترون میتواند تنها ساعتگرد (s=-1/2) و یا پادساعتگرد (s=+1/2) چرخش کند. در شکل زیر چرخش الکترون در این دو حالت نشان داده شده است.
همانطور که بیان شد هر اوربیتال دارای شکل مشخصی است که با توجه به اعداد کوانتومی معلوم میشوند. در ادامه اعداد کوانتومی مرتبط با هر اوبیتال و نحوه قرار گرفتن الکترونها در اوربیتالها را بیان خواهیم کرد.
در هر لایه یا به عبارتی در هر n، تعداد n-1 اوربیتال متفاوت میتواند قرار گیرد. برای نمونه در لایه اول تنها اوربیتال l=0 یا همان اوربیتال کروی وجود دارد. در n=2 دو اوربیتالِ کرویِ (l=0) و دمبلی (l=1) میتوانند قرار گیرند. از طرفی اوربیتال کروی تنها به یک شکل میتواند در فضا قرار گیرد، از این رو m آن تنها برابر با ۰ میتواند باشد. این در حالی است که اوربیتال دمبلی به ۳ شکل میتواند در فضا قرار گیرد، در نتیجه m=-1,0,+1 است. شکل زیر دو اوربیتال s و p را نشان میدهد.
به همین صورت اعداد هر اوربیتال معلوم میشوند. برای نمونه اوربیتال p (یا همان دمبلی) را در نظر بگیرید که در لایه سوم قرار گرفته است. برای این اوربیتال اعداد کوانتومی بهصورت زیر هستند.
توجه داشته باشید که عدد کوانتومی اسپینی برای یک الکترون تعریف میشود، به همین دلیل این عدد در بالا ارائه نشده. اوربیتالهای با l=1 (اوربیتال p) به بالا دارای شکلهایی بسیار پیچیده هستند که بهصورت گوناگونی میتوانند در فضا قرار گیرند. در جدول زیر ترتیب لایهها و زیرلایهها (اوربیتالها) برای چهار لایه اول ارائه شده است.
در جدول بالا ستونی تحت عنوان تعداد الکترونها وجود دارد. این ستون ظرفیت تعداد الکترونهای قرار گرفته در هر اوربیتال را نشان میدهد. برای نمونه اوربیتال p در سه جهت میتواند در فضا قرار گیرد. از طرفی در هرکدام از این حالات ۲ الکترون میتواند در اوربیتال مذکور وجود داشته باشد؛ بنابراین ظرفیت این اوربیتال برابر با ۶=۳×۲ است. البته ظرفیت هر اوربیتال با عدد L را میتوان با استفاده از فرمولِ $$2(2L+1)$$ نیز بدست آورد.
در تصویر زیر، شکل اوربیتالهای s,p,d,f نشان داده شده.
الکترونهای یک اتم با نظم مشخصی در اوربیتالها قرار میگیرند. در ابتدا لایههای با انرژی کمتر توسط الکترونها پر شده و پس از آن لایههای دورتر توسط آنها اشغال میشوند. با استفاده از «اصل آفبا» (Aufbau Principle) میتوان ترتیب الکترونها را در پر کردن اوربیتالها معلوم کرد.
در این اصل در ابتدا لایه با n کمتر توسط الکترونها اشغال میشوند. همچنین در یک لایه، ابتدا اوربیتال با انرژی کمتر پر میشود. برای نمونه در لایه دوم هر دو اوربیتالِ p و s وجود دارند. اما با توجه به انرژی کمتر اوربیتال s، در ابتدا این اوربیتال پر میشود. اما گاهی اوربیتال p در لایهای پایینتر به نسبت اوربیتال s قرار دارد. به نظر شما در این حالت اولویت با شماره لایه یا شکل اوربیتال است؟ در این حالت لایهای زودتر پر میشود که:
بر اساس دو الگوی بالا، الکترونها بهترتیب در اوربیتالهای زیر قرار میگیرند:
همانطور که در فرمول بالا میبینید در ابتدا شماره لایه و پس از آن حرف مربوط به زیرلایه (یا همان اوربیتال) نوشته میشود. البته بهمنظور به خاطر سپردنِ عبارت فوق میتوانید از تصویر زیر نیز استفاده کنید.
همانطور که در بالا نیز بیان شد، هر اوربیتال میتواند $$2(2L+1)$$ الکترون را در خود نگه دارد. برای نوشتن آرایش الکترونی یک اتم میتوان بهترتیب پر شدن، اوربیتالها را نوشت. در بالای هر اوربیتال ظرفیت مربوط به آن نوشته میشود. در ادامه آرایش الکترونی چندین اتم برای نمونه ارائه شدهاند. البته بعضی مواقع اوربیتالها را بهصورت مربع نشان میدهند. همچنین الکترونها را با فلشهایی نمایش میدهند که جهت آن، اسپین الکترون را نشان میدهد. جهت درک بهتر به مثالهای زیر توجه فرمایید. نمادهای استفاده شده در نوشتن آرایش الکترونی مطابق با الگوی زیر تعریف میشوند.
آرایش الکترونی اتم لیتیوم به چه صورت است؟
همانطور که احتمالا میدانید عدد اتمی لیتیوم، ۳ در نتیجه مجموع الکترونهای اشغال شده در اوربیتالهایش نیز برابر با ۳ است؛ مطابق با اصل آفبا، آرایش الکترونی اتم لیتیوم بهصورت زیر خواهد بود.
همانطور که میبینید در لایه اول اوربیتال s پر شده، اما در لایه دوم تنها یک الکترون در اوربیتال s قرار گرفته است. توجه داشته باشید که جهت بالا و پایین، جهت چرخش الکترون دور خودش -یا همان اسپین- را نشان میدهد.
آرایش الکترونی اتم کربن به چه شکل است؟
عدد اتمی کربن برابر با ۶ است. در نتیجه مجموع الکترونهای موجود در اوربیتالها بایستی برابر با ۶ باشد. توجه داشته باشید که در ابتدا یک اوربیتال بایستی پر شده و سپس اوربیتال بعدی را پر کنید. در زیر آرایش الکترونی اتم کربن رسم شده.
در آرایش بالا هر خانه نشان دهنده یک جهت از اوربیتال است. با توجه به اینکه اوربیتال p به ۳ شکل در فضا قرار میگیرد، بنابراین از سه خانه برای نشان دادن آن استفاده شده است. بهمنظور رسم فلشها، از چپ به راست در هر خانه یک فلش رو به بالا قرار داده و به همین شکل اوربیتال را پر کنید. مجموعِ کل فلشها بایستی برابر با عدد اتمی اتمِ مذکور باشد. پیشنهاد میکنیم چندین آرایش الکترونی را برای اتمهای مختلف نوشته و صحت آن با توجه به جدول زیر مورد بررسی قرار دهید.
البته با توجه به پایدار بودن عناصر نجیب، میتوان با استفاده از آنها نیز آرایش الکترونی را بیان کرد. برای نمونه در زیر آرایش الکترونی اتم کربن بر اساس آرایش هلیوم ارائه شده است.
توجه داشته باشید که به منظور نوشتن آرایش الکترونی یونها، عدد اتمی برابر با تعداد الکترونها نیست. برای نمونه در زیر آرایش الکترونی اتم آهن (Fe) و در نتیجه یونِ آهن (2+Fe) ارائه شده است.
در صورت علاقهمندی به مباحث مرتبط در زمینه فیزیک و شیمی، آموزشهای زیر نیز به شما پیشنهاد میشوند:
چگونه آرایش الکترونی بنویسیم
^^
مجید عوض زاده (+)
«مجید عوضزاده»، فارغ التحصیل مقطع کارشناسی ارشد رشته مهندسی مکانیک از دانشگاه تهران است. فیزیک، ریاضیات و مهندسی مکانیک از جمله مباحث مورد علاقه او هستند که در رابطه با آنها تولید محتوا میکند.
بر اساس رای 195 نفر
آیا این مطلب برای شما مفید بود؟
واقن فوق العاده درس دادین این مطلبو و کامل یادگرفتم
دستتون درد نکنه واقن مرسی بابت زحماتی ک میکشید .
دمتون گرم
سر کلاس استاد که چیزی نفهمیدم. اما اینجا همه چیز رو متوجه شدم عالی.
لینک مطلب رو برای دوستام هم فرستادم
دستتون درد نکنه
به نام خدا
با سلام و عرض ادب و احترام
برای شما از خداوند متعال آرزوی موفقیت روزافزون دارم. بسیار ممنون، زحمت کشیدید و مطالب مفیدی ارائه دادید.
واقعا درسی ک اقای بهنام محمدیان میدن بهترین و عالیترینه و کاملا بی نقصه و من کلا درسو یاد میگیرم
ب امید موفقیت های بیشتررررررر …ممنونم ازتون
خیلی عالی بود.
ممنونم
بعد از سال ها فاصله گرفتن از شیمی دبیرستان، این مطلب به خوبی، خیلی عالی، مطالب رو یادآوری کرد.
ممنون. خیلی خوب بود
خیلی عالی بود بعد از مدت ها یه تدریس خوب واسه این مبحث دیدم🌹
عالی ممنون واقعا خیلی خوب توضیح دادید. فقط اگه میشه توی اموزشاتتون ، انتهای هر اموزش فرمول ها و رابطه ها و مطالب خیلی مهم رو که توضیح داده شده رو یه جا مثلا توی جدول جمع کنین تا دسترسی بهش سریع تر و راحت تر بشه. مثل همون تقلب نامه هایی که منتشر میکنید. بازم ممنون با تشکر از سایت خوبتون.
با سلام. الان برای اوربیتال ۲p طبق شکل هسته در کجای شکل قرار میگیره؟ چون از اونجایی که الکترون به دور هسته می چرخه باید یه شکل کروی داشته باشه و یه مقدار شکل ها غیر عادیه.
مرسی خیلی به من کمک کرد.
خوب ولی کاش با فیلم توضیح میدادید .
بسیار عالی ممنونم
خیلی عالی کامل و بی نقص
تشکرمیکنم ازمجله فرادرس
نشانی ایمیل شما منتشر نخواهد شد. بخشهای موردنیاز علامتگذاری شدهاند *
سازمان علمی و آموزشی «فرادرس» (Faradars) از قدیمیترین وبسایتهای یادگیری آنلاین است که توانسته طی بیش از ده سال فعالیت خود بالغ بر ۱۲۰۰۰ ساعت آموزش ویدیویی در قالب فراتر از ۲۰۰۰ عنوان علمی، مهارتی و کاربردی را منتشر کند و به بزرگترین پلتفرم آموزشی ایران مبدل شود.
فرادرس با پایبندی به شعار «دانش در دسترس همه، همیشه و همه جا» با همکاری بیش از ۱۸۰۰ مدرس برجسته در زمینههای علمی گوناگون از جمله آمار و دادهکاوی، هوش مصنوعی، برنامهنویسی، طراحی و گرافیک کامپیوتری، آموزشهای دانشگاهی و تخصصی، آموزش نرمافزارهای گوناگون، دروس رسمی دبیرستان و پیش دانشگاهی، آموزشهای دانشآموزی و نوجوانان، آموزش زبانهای خارجی، مهندسی برق، الکترونیک و رباتیک، مهندسی کنترل، مهندسی مکانیک، مهندسی شیمی، مهندسی صنایع، مهندسی معماری و مهندسی عمران توانسته بستری را فراهم کند تا افراد با شرایط مختلف زمانی، مکانی و جسمانی بتوانند با بهرهگیری از آموزشهای با کیفیت، به روز و مهارتمحور همواره به یادگیری بپردازند. شما هم با پیوستن به جمع بزرگ و بالغ بر ۶۰۰ هزار نفری دانشجویان و دانشآموزان فرادرس و با بهرهگیری از آموزشهای آن، میتوانید تجربهای متفاوت از علم و مهارتآموزی داشته باشید.
مشاهده بیشتر
هر گونه بهرهگیری از مطالب مجله فرادرس به معنی پذیرش شرایط استفاده از آن بوده و کپی بخش یا کل هر کدام از مطالب، تنها با کسب مجوز مکتوب امکان پذیر است.
© فرادرس ۱۳۹۹
پیشتر در وبلاگ فرادرس مدل اتمی بور را توضیح دادیم. مدل اتمی بور مدلی یکبعدی است که تنها از یک عدد جهت توصیف الکترونهای یک اتم استفاده میکند. این عدد همان n است که نشان دهنده لایهای است که الکترون در آن میچرخد. همچنین مدل مذکور تنها میتواند ویژگیهای اتم هیدروژن را توجیه کند.
محتوای این مطلب جهت یادگیری بهتر و سریعتر آن، در انتهای متن به صورت ویدیویی نیز ارائه شده است.
«اروین شرودینگر» (Erwin Schrödinger)، در سال ۱۹۲۶ با استفاده از محاسبات پیچیده ریاضی نشان داد که الکترونهای یک اتم در مسیرهایی سهبعدی حرکت میکنند؛ از این رو به سه عدد جهت توصیف الکترونها نیازمندیم. البته به عدد چهارمی نیز بهمنظور نشان دادن نحوه حرکت الکترون به دور خودش نیازمند هستیم. هر الکترون در فضایی ابری تحت عنوان اوربیتال در حال حرکت است. نحوه این حرکت و آرایش الکترونها در شکلگیری پیوندهای شیمیایی بسیار تاثیرگذار هستند. با استفاده از اعداد کوانتومی که در ادامه به آنها خواهیم پرداخت، میتوان اوربیتالها را به شکلی دقیقتر توصیف کرد.
شرودینگر با حل معادلاتش سه عدد را جهت توصیف الکترونهای یک اتم ارائه داد. این اعداد عبارتند از:
عدد کوانتومی اصلی یا n، نشان دهنده اندازه و انرژی اوربیتال است. منظور از اندازه اوربیتال، فاصله الکترونها از هسته اتم است. هرچه اندازه این عدد بیشتر باشد، اندازه و انرژی اوربیتال نیز بزرگتر خواهد بود. تمامی الکترونهایی که n آنها با هم برابر است، در فاصلهای یکسان از هسته اتم قرار میگیرند.
چگونه آرایش الکترونی بنویسیم
L یا عدد کوانتومی فرعی، نشاندهنده شکل اوربیتال است. یک لایه با عدد کوانتومی n میتواند از n-1 اوربیتال مختلف تشکیل شده باشد. شکلهای یک اوربیتال را با نمادهای $$s,p,d,f,…$$ نشان میدهند. برای نمونه L=۰ نشان دهنده اوربیتال s یا L=۱ اوربیتال p را نشان میدهد. تصویر ارائه شده، شکل اوربیتالهای مختلف را نمایش میدهد.
با توجه به شکل فوق، اوربیتال s کروی بوده و تنها به یک صورت میتواند در فضا قرار گیرد. اما مثلا اوربیتال p میتواند هم در راستای محور z و هم در راستای محور x جهتگیری کند. از این رو به عدد سومی تحت عنوان m یا عدد کوانتومی مغناطیسی نیازمندیم تا این جهتگیری اوربیتالها را نشان دهیم. بنابراین عدد m جهتگیری اوربیتال را در فضا نشان میدهد. عدد کوانتومی مغناطیسیِ یک اوربیتال، بین L- و L+ قرار دارد. برای نمونه اعداد کوانتومی مغناطیسی برای اوربیتال p که L مربوط با آن ۱ است، برابر با 1+,1,0- در نظر گرفته میشوند.
اگر الکترون را به صورت یک کره در نظر بگیریم، با استفاده از ۳ عدد معرفی شده در بالا میتواند جهت حرکت آن را در فضا مشخص کرد. اما این الکترون، به دور خودش نیز در حال چرخش است. این چرخش را با عدد کوانتومی اسپینی یا ms نشان میدهند. بنابراین یک الکترون میتواند تنها ساعتگرد (s=-1/2) و یا پادساعتگرد (s=+1/2) چرخش کند. در شکل زیر چرخش الکترون در این دو حالت نشان داده شده است.
همانطور که بیان شد هر اوربیتال دارای شکل مشخصی است که با توجه به اعداد کوانتومی معلوم میشوند. در ادامه اعداد کوانتومی مرتبط با هر اوبیتال و نحوه قرار گرفتن الکترونها در اوربیتالها را بیان خواهیم کرد.
در هر لایه یا به عبارتی در هر n، تعداد n-1 اوربیتال متفاوت میتواند قرار گیرد. برای نمونه در لایه اول تنها اوربیتال l=0 یا همان اوربیتال کروی وجود دارد. در n=2 دو اوربیتالِ کرویِ (l=0) و دمبلی (l=1) میتوانند قرار گیرند. از طرفی اوربیتال کروی تنها به یک شکل میتواند در فضا قرار گیرد، از این رو m آن تنها برابر با ۰ میتواند باشد. این در حالی است که اوربیتال دمبلی به ۳ شکل میتواند در فضا قرار گیرد، در نتیجه m=-1,0,+1 است. شکل زیر دو اوربیتال s و p را نشان میدهد.
به همین صورت اعداد هر اوربیتال معلوم میشوند. برای نمونه اوربیتال p (یا همان دمبلی) را در نظر بگیرید که در لایه سوم قرار گرفته است. برای این اوربیتال اعداد کوانتومی بهصورت زیر هستند.
توجه داشته باشید که عدد کوانتومی اسپینی برای یک الکترون تعریف میشود، به همین دلیل این عدد در بالا ارائه نشده. اوربیتالهای با l=1 (اوربیتال p) به بالا دارای شکلهایی بسیار پیچیده هستند که بهصورت گوناگونی میتوانند در فضا قرار گیرند. در جدول زیر ترتیب لایهها و زیرلایهها (اوربیتالها) برای چهار لایه اول ارائه شده است.
در جدول بالا ستونی تحت عنوان تعداد الکترونها وجود دارد. این ستون ظرفیت تعداد الکترونهای قرار گرفته در هر اوربیتال را نشان میدهد. برای نمونه اوربیتال p در سه جهت میتواند در فضا قرار گیرد. از طرفی در هرکدام از این حالات ۲ الکترون میتواند در اوربیتال مذکور وجود داشته باشد؛ بنابراین ظرفیت این اوربیتال برابر با ۶=۳×۲ است. البته ظرفیت هر اوربیتال با عدد L را میتوان با استفاده از فرمولِ $$2(2L+1)$$ نیز بدست آورد.
در تصویر زیر، شکل اوربیتالهای s,p,d,f نشان داده شده.
الکترونهای یک اتم با نظم مشخصی در اوربیتالها قرار میگیرند. در ابتدا لایههای با انرژی کمتر توسط الکترونها پر شده و پس از آن لایههای دورتر توسط آنها اشغال میشوند. با استفاده از «اصل آفبا» (Aufbau Principle) میتوان ترتیب الکترونها را در پر کردن اوربیتالها معلوم کرد.
در این اصل در ابتدا لایه با n کمتر توسط الکترونها اشغال میشوند. همچنین در یک لایه، ابتدا اوربیتال با انرژی کمتر پر میشود. برای نمونه در لایه دوم هر دو اوربیتالِ p و s وجود دارند. اما با توجه به انرژی کمتر اوربیتال s، در ابتدا این اوربیتال پر میشود. اما گاهی اوربیتال p در لایهای پایینتر به نسبت اوربیتال s قرار دارد. به نظر شما در این حالت اولویت با شماره لایه یا شکل اوربیتال است؟ در این حالت لایهای زودتر پر میشود که:
بر اساس دو الگوی بالا، الکترونها بهترتیب در اوربیتالهای زیر قرار میگیرند:
همانطور که در فرمول بالا میبینید در ابتدا شماره لایه و پس از آن حرف مربوط به زیرلایه (یا همان اوربیتال) نوشته میشود. البته بهمنظور به خاطر سپردنِ عبارت فوق میتوانید از تصویر زیر نیز استفاده کنید.
همانطور که در بالا نیز بیان شد، هر اوربیتال میتواند $$2(2L+1)$$ الکترون را در خود نگه دارد. برای نوشتن آرایش الکترونی یک اتم میتوان بهترتیب پر شدن، اوربیتالها را نوشت. در بالای هر اوربیتال ظرفیت مربوط به آن نوشته میشود. در ادامه آرایش الکترونی چندین اتم برای نمونه ارائه شدهاند. البته بعضی مواقع اوربیتالها را بهصورت مربع نشان میدهند. همچنین الکترونها را با فلشهایی نمایش میدهند که جهت آن، اسپین الکترون را نشان میدهد. جهت درک بهتر به مثالهای زیر توجه فرمایید. نمادهای استفاده شده در نوشتن آرایش الکترونی مطابق با الگوی زیر تعریف میشوند.
آرایش الکترونی اتم لیتیوم به چه صورت است؟
همانطور که احتمالا میدانید عدد اتمی لیتیوم، ۳ در نتیجه مجموع الکترونهای اشغال شده در اوربیتالهایش نیز برابر با ۳ است؛ مطابق با اصل آفبا، آرایش الکترونی اتم لیتیوم بهصورت زیر خواهد بود.
همانطور که میبینید در لایه اول اوربیتال s پر شده، اما در لایه دوم تنها یک الکترون در اوربیتال s قرار گرفته است. توجه داشته باشید که جهت بالا و پایین، جهت چرخش الکترون دور خودش -یا همان اسپین- را نشان میدهد.
آرایش الکترونی اتم کربن به چه شکل است؟
عدد اتمی کربن برابر با ۶ است. در نتیجه مجموع الکترونهای موجود در اوربیتالها بایستی برابر با ۶ باشد. توجه داشته باشید که در ابتدا یک اوربیتال بایستی پر شده و سپس اوربیتال بعدی را پر کنید. در زیر آرایش الکترونی اتم کربن رسم شده.
در آرایش بالا هر خانه نشان دهنده یک جهت از اوربیتال است. با توجه به اینکه اوربیتال p به ۳ شکل در فضا قرار میگیرد، بنابراین از سه خانه برای نشان دادن آن استفاده شده است. بهمنظور رسم فلشها، از چپ به راست در هر خانه یک فلش رو به بالا قرار داده و به همین شکل اوربیتال را پر کنید. مجموعِ کل فلشها بایستی برابر با عدد اتمی اتمِ مذکور باشد. پیشنهاد میکنیم چندین آرایش الکترونی را برای اتمهای مختلف نوشته و صحت آن با توجه به جدول زیر مورد بررسی قرار دهید.
البته با توجه به پایدار بودن عناصر نجیب، میتوان با استفاده از آنها نیز آرایش الکترونی را بیان کرد. برای نمونه در زیر آرایش الکترونی اتم کربن بر اساس آرایش هلیوم ارائه شده است.
توجه داشته باشید که به منظور نوشتن آرایش الکترونی یونها، عدد اتمی برابر با تعداد الکترونها نیست. برای نمونه در زیر آرایش الکترونی اتم آهن (Fe) و در نتیجه یونِ آهن (2+Fe) ارائه شده است.
در صورت علاقهمندی به مباحث مرتبط در زمینه فیزیک و شیمی، آموزشهای زیر نیز به شما پیشنهاد میشوند:
چگونه آرایش الکترونی بنویسیم
^^
مجید عوض زاده (+)
«مجید عوضزاده»، فارغ التحصیل مقطع کارشناسی ارشد رشته مهندسی مکانیک از دانشگاه تهران است. فیزیک، ریاضیات و مهندسی مکانیک از جمله مباحث مورد علاقه او هستند که در رابطه با آنها تولید محتوا میکند.
بر اساس رای 195 نفر
آیا این مطلب برای شما مفید بود؟
واقن فوق العاده درس دادین این مطلبو و کامل یادگرفتم
دستتون درد نکنه واقن مرسی بابت زحماتی ک میکشید .
دمتون گرم
سر کلاس استاد که چیزی نفهمیدم. اما اینجا همه چیز رو متوجه شدم عالی.
لینک مطلب رو برای دوستام هم فرستادم
دستتون درد نکنه
به نام خدا
با سلام و عرض ادب و احترام
برای شما از خداوند متعال آرزوی موفقیت روزافزون دارم. بسیار ممنون، زحمت کشیدید و مطالب مفیدی ارائه دادید.
واقعا درسی ک اقای بهنام محمدیان میدن بهترین و عالیترینه و کاملا بی نقصه و من کلا درسو یاد میگیرم
ب امید موفقیت های بیشتررررررر …ممنونم ازتون
خیلی عالی بود.
ممنونم
بعد از سال ها فاصله گرفتن از شیمی دبیرستان، این مطلب به خوبی، خیلی عالی، مطالب رو یادآوری کرد.
ممنون. خیلی خوب بود
خیلی عالی بود بعد از مدت ها یه تدریس خوب واسه این مبحث دیدم🌹
عالی ممنون واقعا خیلی خوب توضیح دادید. فقط اگه میشه توی اموزشاتتون ، انتهای هر اموزش فرمول ها و رابطه ها و مطالب خیلی مهم رو که توضیح داده شده رو یه جا مثلا توی جدول جمع کنین تا دسترسی بهش سریع تر و راحت تر بشه. مثل همون تقلب نامه هایی که منتشر میکنید. بازم ممنون با تشکر از سایت خوبتون.
با سلام. الان برای اوربیتال ۲p طبق شکل هسته در کجای شکل قرار میگیره؟ چون از اونجایی که الکترون به دور هسته می چرخه باید یه شکل کروی داشته باشه و یه مقدار شکل ها غیر عادیه.
مرسی خیلی به من کمک کرد.
خوب ولی کاش با فیلم توضیح میدادید .
بسیار عالی ممنونم
خیلی عالی کامل و بی نقص
تشکرمیکنم ازمجله فرادرس
نشانی ایمیل شما منتشر نخواهد شد. بخشهای موردنیاز علامتگذاری شدهاند *
سازمان علمی و آموزشی «فرادرس» (Faradars) از قدیمیترین وبسایتهای یادگیری آنلاین است که توانسته طی بیش از ده سال فعالیت خود بالغ بر ۱۲۰۰۰ ساعت آموزش ویدیویی در قالب فراتر از ۲۰۰۰ عنوان علمی، مهارتی و کاربردی را منتشر کند و به بزرگترین پلتفرم آموزشی ایران مبدل شود.
فرادرس با پایبندی به شعار «دانش در دسترس همه، همیشه و همه جا» با همکاری بیش از ۱۸۰۰ مدرس برجسته در زمینههای علمی گوناگون از جمله آمار و دادهکاوی، هوش مصنوعی، برنامهنویسی، طراحی و گرافیک کامپیوتری، آموزشهای دانشگاهی و تخصصی، آموزش نرمافزارهای گوناگون، دروس رسمی دبیرستان و پیش دانشگاهی، آموزشهای دانشآموزی و نوجوانان، آموزش زبانهای خارجی، مهندسی برق، الکترونیک و رباتیک، مهندسی کنترل، مهندسی مکانیک، مهندسی شیمی، مهندسی صنایع، مهندسی معماری و مهندسی عمران توانسته بستری را فراهم کند تا افراد با شرایط مختلف زمانی، مکانی و جسمانی بتوانند با بهرهگیری از آموزشهای با کیفیت، به روز و مهارتمحور همواره به یادگیری بپردازند. شما هم با پیوستن به جمع بزرگ و بالغ بر ۶۰۰ هزار نفری دانشجویان و دانشآموزان فرادرس و با بهرهگیری از آموزشهای آن، میتوانید تجربهای متفاوت از علم و مهارتآموزی داشته باشید.
مشاهده بیشتر
هر گونه بهرهگیری از مطالب مجله فرادرس به معنی پذیرش شرایط استفاده از آن بوده و کپی بخش یا کل هر کدام از مطالب، تنها با کسب مجوز مکتوب امکان پذیر است.
© فرادرس ۱۳۹۹
پیشتر در وبلاگ فرادرس مدل اتمی بور را توضیح دادیم. مدل اتمی بور مدلی یکبعدی است که تنها از یک عدد جهت توصیف الکترونهای یک اتم استفاده میکند. این عدد همان n است که نشان دهنده لایهای است که الکترون در آن میچرخد. همچنین مدل مذکور تنها میتواند ویژگیهای اتم هیدروژن را توجیه کند.
محتوای این مطلب جهت یادگیری بهتر و سریعتر آن، در انتهای متن به صورت ویدیویی نیز ارائه شده است.
«اروین شرودینگر» (Erwin Schrödinger)، در سال ۱۹۲۶ با استفاده از محاسبات پیچیده ریاضی نشان داد که الکترونهای یک اتم در مسیرهایی سهبعدی حرکت میکنند؛ از این رو به سه عدد جهت توصیف الکترونها نیازمندیم. البته به عدد چهارمی نیز بهمنظور نشان دادن نحوه حرکت الکترون به دور خودش نیازمند هستیم. هر الکترون در فضایی ابری تحت عنوان اوربیتال در حال حرکت است. نحوه این حرکت و آرایش الکترونها در شکلگیری پیوندهای شیمیایی بسیار تاثیرگذار هستند. با استفاده از اعداد کوانتومی که در ادامه به آنها خواهیم پرداخت، میتوان اوربیتالها را به شکلی دقیقتر توصیف کرد.
شرودینگر با حل معادلاتش سه عدد را جهت توصیف الکترونهای یک اتم ارائه داد. این اعداد عبارتند از:
عدد کوانتومی اصلی یا n، نشان دهنده اندازه و انرژی اوربیتال است. منظور از اندازه اوربیتال، فاصله الکترونها از هسته اتم است. هرچه اندازه این عدد بیشتر باشد، اندازه و انرژی اوربیتال نیز بزرگتر خواهد بود. تمامی الکترونهایی که n آنها با هم برابر است، در فاصلهای یکسان از هسته اتم قرار میگیرند.
چگونه آرایش الکترونی بنویسیم
L یا عدد کوانتومی فرعی، نشاندهنده شکل اوربیتال است. یک لایه با عدد کوانتومی n میتواند از n-1 اوربیتال مختلف تشکیل شده باشد. شکلهای یک اوربیتال را با نمادهای $$s,p,d,f,…$$ نشان میدهند. برای نمونه L=۰ نشان دهنده اوربیتال s یا L=۱ اوربیتال p را نشان میدهد. تصویر ارائه شده، شکل اوربیتالهای مختلف را نمایش میدهد.
با توجه به شکل فوق، اوربیتال s کروی بوده و تنها به یک صورت میتواند در فضا قرار گیرد. اما مثلا اوربیتال p میتواند هم در راستای محور z و هم در راستای محور x جهتگیری کند. از این رو به عدد سومی تحت عنوان m یا عدد کوانتومی مغناطیسی نیازمندیم تا این جهتگیری اوربیتالها را نشان دهیم. بنابراین عدد m جهتگیری اوربیتال را در فضا نشان میدهد. عدد کوانتومی مغناطیسیِ یک اوربیتال، بین L- و L+ قرار دارد. برای نمونه اعداد کوانتومی مغناطیسی برای اوربیتال p که L مربوط با آن ۱ است، برابر با 1+,1,0- در نظر گرفته میشوند.
اگر الکترون را به صورت یک کره در نظر بگیریم، با استفاده از ۳ عدد معرفی شده در بالا میتواند جهت حرکت آن را در فضا مشخص کرد. اما این الکترون، به دور خودش نیز در حال چرخش است. این چرخش را با عدد کوانتومی اسپینی یا ms نشان میدهند. بنابراین یک الکترون میتواند تنها ساعتگرد (s=-1/2) و یا پادساعتگرد (s=+1/2) چرخش کند. در شکل زیر چرخش الکترون در این دو حالت نشان داده شده است.
همانطور که بیان شد هر اوربیتال دارای شکل مشخصی است که با توجه به اعداد کوانتومی معلوم میشوند. در ادامه اعداد کوانتومی مرتبط با هر اوبیتال و نحوه قرار گرفتن الکترونها در اوربیتالها را بیان خواهیم کرد.
در هر لایه یا به عبارتی در هر n، تعداد n-1 اوربیتال متفاوت میتواند قرار گیرد. برای نمونه در لایه اول تنها اوربیتال l=0 یا همان اوربیتال کروی وجود دارد. در n=2 دو اوربیتالِ کرویِ (l=0) و دمبلی (l=1) میتوانند قرار گیرند. از طرفی اوربیتال کروی تنها به یک شکل میتواند در فضا قرار گیرد، از این رو m آن تنها برابر با ۰ میتواند باشد. این در حالی است که اوربیتال دمبلی به ۳ شکل میتواند در فضا قرار گیرد، در نتیجه m=-1,0,+1 است. شکل زیر دو اوربیتال s و p را نشان میدهد.
به همین صورت اعداد هر اوربیتال معلوم میشوند. برای نمونه اوربیتال p (یا همان دمبلی) را در نظر بگیرید که در لایه سوم قرار گرفته است. برای این اوربیتال اعداد کوانتومی بهصورت زیر هستند.
توجه داشته باشید که عدد کوانتومی اسپینی برای یک الکترون تعریف میشود، به همین دلیل این عدد در بالا ارائه نشده. اوربیتالهای با l=1 (اوربیتال p) به بالا دارای شکلهایی بسیار پیچیده هستند که بهصورت گوناگونی میتوانند در فضا قرار گیرند. در جدول زیر ترتیب لایهها و زیرلایهها (اوربیتالها) برای چهار لایه اول ارائه شده است.
در جدول بالا ستونی تحت عنوان تعداد الکترونها وجود دارد. این ستون ظرفیت تعداد الکترونهای قرار گرفته در هر اوربیتال را نشان میدهد. برای نمونه اوربیتال p در سه جهت میتواند در فضا قرار گیرد. از طرفی در هرکدام از این حالات ۲ الکترون میتواند در اوربیتال مذکور وجود داشته باشد؛ بنابراین ظرفیت این اوربیتال برابر با ۶=۳×۲ است. البته ظرفیت هر اوربیتال با عدد L را میتوان با استفاده از فرمولِ $$2(2L+1)$$ نیز بدست آورد.
در تصویر زیر، شکل اوربیتالهای s,p,d,f نشان داده شده.
الکترونهای یک اتم با نظم مشخصی در اوربیتالها قرار میگیرند. در ابتدا لایههای با انرژی کمتر توسط الکترونها پر شده و پس از آن لایههای دورتر توسط آنها اشغال میشوند. با استفاده از «اصل آفبا» (Aufbau Principle) میتوان ترتیب الکترونها را در پر کردن اوربیتالها معلوم کرد.
در این اصل در ابتدا لایه با n کمتر توسط الکترونها اشغال میشوند. همچنین در یک لایه، ابتدا اوربیتال با انرژی کمتر پر میشود. برای نمونه در لایه دوم هر دو اوربیتالِ p و s وجود دارند. اما با توجه به انرژی کمتر اوربیتال s، در ابتدا این اوربیتال پر میشود. اما گاهی اوربیتال p در لایهای پایینتر به نسبت اوربیتال s قرار دارد. به نظر شما در این حالت اولویت با شماره لایه یا شکل اوربیتال است؟ در این حالت لایهای زودتر پر میشود که:
بر اساس دو الگوی بالا، الکترونها بهترتیب در اوربیتالهای زیر قرار میگیرند:
همانطور که در فرمول بالا میبینید در ابتدا شماره لایه و پس از آن حرف مربوط به زیرلایه (یا همان اوربیتال) نوشته میشود. البته بهمنظور به خاطر سپردنِ عبارت فوق میتوانید از تصویر زیر نیز استفاده کنید.
همانطور که در بالا نیز بیان شد، هر اوربیتال میتواند $$2(2L+1)$$ الکترون را در خود نگه دارد. برای نوشتن آرایش الکترونی یک اتم میتوان بهترتیب پر شدن، اوربیتالها را نوشت. در بالای هر اوربیتال ظرفیت مربوط به آن نوشته میشود. در ادامه آرایش الکترونی چندین اتم برای نمونه ارائه شدهاند. البته بعضی مواقع اوربیتالها را بهصورت مربع نشان میدهند. همچنین الکترونها را با فلشهایی نمایش میدهند که جهت آن، اسپین الکترون را نشان میدهد. جهت درک بهتر به مثالهای زیر توجه فرمایید. نمادهای استفاده شده در نوشتن آرایش الکترونی مطابق با الگوی زیر تعریف میشوند.
آرایش الکترونی اتم لیتیوم به چه صورت است؟
همانطور که احتمالا میدانید عدد اتمی لیتیوم، ۳ در نتیجه مجموع الکترونهای اشغال شده در اوربیتالهایش نیز برابر با ۳ است؛ مطابق با اصل آفبا، آرایش الکترونی اتم لیتیوم بهصورت زیر خواهد بود.
همانطور که میبینید در لایه اول اوربیتال s پر شده، اما در لایه دوم تنها یک الکترون در اوربیتال s قرار گرفته است. توجه داشته باشید که جهت بالا و پایین، جهت چرخش الکترون دور خودش -یا همان اسپین- را نشان میدهد.
آرایش الکترونی اتم کربن به چه شکل است؟
عدد اتمی کربن برابر با ۶ است. در نتیجه مجموع الکترونهای موجود در اوربیتالها بایستی برابر با ۶ باشد. توجه داشته باشید که در ابتدا یک اوربیتال بایستی پر شده و سپس اوربیتال بعدی را پر کنید. در زیر آرایش الکترونی اتم کربن رسم شده.
در آرایش بالا هر خانه نشان دهنده یک جهت از اوربیتال است. با توجه به اینکه اوربیتال p به ۳ شکل در فضا قرار میگیرد، بنابراین از سه خانه برای نشان دادن آن استفاده شده است. بهمنظور رسم فلشها، از چپ به راست در هر خانه یک فلش رو به بالا قرار داده و به همین شکل اوربیتال را پر کنید. مجموعِ کل فلشها بایستی برابر با عدد اتمی اتمِ مذکور باشد. پیشنهاد میکنیم چندین آرایش الکترونی را برای اتمهای مختلف نوشته و صحت آن با توجه به جدول زیر مورد بررسی قرار دهید.
البته با توجه به پایدار بودن عناصر نجیب، میتوان با استفاده از آنها نیز آرایش الکترونی را بیان کرد. برای نمونه در زیر آرایش الکترونی اتم کربن بر اساس آرایش هلیوم ارائه شده است.
توجه داشته باشید که به منظور نوشتن آرایش الکترونی یونها، عدد اتمی برابر با تعداد الکترونها نیست. برای نمونه در زیر آرایش الکترونی اتم آهن (Fe) و در نتیجه یونِ آهن (2+Fe) ارائه شده است.
در صورت علاقهمندی به مباحث مرتبط در زمینه فیزیک و شیمی، آموزشهای زیر نیز به شما پیشنهاد میشوند:
چگونه آرایش الکترونی بنویسیم
^^
مجید عوض زاده (+)
«مجید عوضزاده»، فارغ التحصیل مقطع کارشناسی ارشد رشته مهندسی مکانیک از دانشگاه تهران است. فیزیک، ریاضیات و مهندسی مکانیک از جمله مباحث مورد علاقه او هستند که در رابطه با آنها تولید محتوا میکند.
بر اساس رای 195 نفر
آیا این مطلب برای شما مفید بود؟
واقن فوق العاده درس دادین این مطلبو و کامل یادگرفتم
دستتون درد نکنه واقن مرسی بابت زحماتی ک میکشید .
دمتون گرم
سر کلاس استاد که چیزی نفهمیدم. اما اینجا همه چیز رو متوجه شدم عالی.
لینک مطلب رو برای دوستام هم فرستادم
دستتون درد نکنه
به نام خدا
با سلام و عرض ادب و احترام
برای شما از خداوند متعال آرزوی موفقیت روزافزون دارم. بسیار ممنون، زحمت کشیدید و مطالب مفیدی ارائه دادید.
واقعا درسی ک اقای بهنام محمدیان میدن بهترین و عالیترینه و کاملا بی نقصه و من کلا درسو یاد میگیرم
ب امید موفقیت های بیشتررررررر …ممنونم ازتون
خیلی عالی بود.
ممنونم
بعد از سال ها فاصله گرفتن از شیمی دبیرستان، این مطلب به خوبی، خیلی عالی، مطالب رو یادآوری کرد.
ممنون. خیلی خوب بود
خیلی عالی بود بعد از مدت ها یه تدریس خوب واسه این مبحث دیدم🌹
عالی ممنون واقعا خیلی خوب توضیح دادید. فقط اگه میشه توی اموزشاتتون ، انتهای هر اموزش فرمول ها و رابطه ها و مطالب خیلی مهم رو که توضیح داده شده رو یه جا مثلا توی جدول جمع کنین تا دسترسی بهش سریع تر و راحت تر بشه. مثل همون تقلب نامه هایی که منتشر میکنید. بازم ممنون با تشکر از سایت خوبتون.
با سلام. الان برای اوربیتال ۲p طبق شکل هسته در کجای شکل قرار میگیره؟ چون از اونجایی که الکترون به دور هسته می چرخه باید یه شکل کروی داشته باشه و یه مقدار شکل ها غیر عادیه.
مرسی خیلی به من کمک کرد.
خوب ولی کاش با فیلم توضیح میدادید .
بسیار عالی ممنونم
خیلی عالی کامل و بی نقص
تشکرمیکنم ازمجله فرادرس
نشانی ایمیل شما منتشر نخواهد شد. بخشهای موردنیاز علامتگذاری شدهاند *
سازمان علمی و آموزشی «فرادرس» (Faradars) از قدیمیترین وبسایتهای یادگیری آنلاین است که توانسته طی بیش از ده سال فعالیت خود بالغ بر ۱۲۰۰۰ ساعت آموزش ویدیویی در قالب فراتر از ۲۰۰۰ عنوان علمی، مهارتی و کاربردی را منتشر کند و به بزرگترین پلتفرم آموزشی ایران مبدل شود.
فرادرس با پایبندی به شعار «دانش در دسترس همه، همیشه و همه جا» با همکاری بیش از ۱۸۰۰ مدرس برجسته در زمینههای علمی گوناگون از جمله آمار و دادهکاوی، هوش مصنوعی، برنامهنویسی، طراحی و گرافیک کامپیوتری، آموزشهای دانشگاهی و تخصصی، آموزش نرمافزارهای گوناگون، دروس رسمی دبیرستان و پیش دانشگاهی، آموزشهای دانشآموزی و نوجوانان، آموزش زبانهای خارجی، مهندسی برق، الکترونیک و رباتیک، مهندسی کنترل، مهندسی مکانیک، مهندسی شیمی، مهندسی صنایع، مهندسی معماری و مهندسی عمران توانسته بستری را فراهم کند تا افراد با شرایط مختلف زمانی، مکانی و جسمانی بتوانند با بهرهگیری از آموزشهای با کیفیت، به روز و مهارتمحور همواره به یادگیری بپردازند. شما هم با پیوستن به جمع بزرگ و بالغ بر ۶۰۰ هزار نفری دانشجویان و دانشآموزان فرادرس و با بهرهگیری از آموزشهای آن، میتوانید تجربهای متفاوت از علم و مهارتآموزی داشته باشید.
مشاهده بیشتر
هر گونه بهرهگیری از مطالب مجله فرادرس به معنی پذیرش شرایط استفاده از آن بوده و کپی بخش یا کل هر کدام از مطالب، تنها با کسب مجوز مکتوب امکان پذیر است.
© فرادرس ۱۳۹۹
پیشتر در وبلاگ فرادرس مدل اتمی بور را توضیح دادیم. مدل اتمی بور مدلی یکبعدی است که تنها از یک عدد جهت توصیف الکترونهای یک اتم استفاده میکند. این عدد همان n است که نشان دهنده لایهای است که الکترون در آن میچرخد. همچنین مدل مذکور تنها میتواند ویژگیهای اتم هیدروژن را توجیه کند.
محتوای این مطلب جهت یادگیری بهتر و سریعتر آن، در انتهای متن به صورت ویدیویی نیز ارائه شده است.
«اروین شرودینگر» (Erwin Schrödinger)، در سال ۱۹۲۶ با استفاده از محاسبات پیچیده ریاضی نشان داد که الکترونهای یک اتم در مسیرهایی سهبعدی حرکت میکنند؛ از این رو به سه عدد جهت توصیف الکترونها نیازمندیم. البته به عدد چهارمی نیز بهمنظور نشان دادن نحوه حرکت الکترون به دور خودش نیازمند هستیم. هر الکترون در فضایی ابری تحت عنوان اوربیتال در حال حرکت است. نحوه این حرکت و آرایش الکترونها در شکلگیری پیوندهای شیمیایی بسیار تاثیرگذار هستند. با استفاده از اعداد کوانتومی که در ادامه به آنها خواهیم پرداخت، میتوان اوربیتالها را به شکلی دقیقتر توصیف کرد.
شرودینگر با حل معادلاتش سه عدد را جهت توصیف الکترونهای یک اتم ارائه داد. این اعداد عبارتند از:
عدد کوانتومی اصلی یا n، نشان دهنده اندازه و انرژی اوربیتال است. منظور از اندازه اوربیتال، فاصله الکترونها از هسته اتم است. هرچه اندازه این عدد بیشتر باشد، اندازه و انرژی اوربیتال نیز بزرگتر خواهد بود. تمامی الکترونهایی که n آنها با هم برابر است، در فاصلهای یکسان از هسته اتم قرار میگیرند.
چگونه آرایش الکترونی بنویسیم
L یا عدد کوانتومی فرعی، نشاندهنده شکل اوربیتال است. یک لایه با عدد کوانتومی n میتواند از n-1 اوربیتال مختلف تشکیل شده باشد. شکلهای یک اوربیتال را با نمادهای $$s,p,d,f,…$$ نشان میدهند. برای نمونه L=۰ نشان دهنده اوربیتال s یا L=۱ اوربیتال p را نشان میدهد. تصویر ارائه شده، شکل اوربیتالهای مختلف را نمایش میدهد.
با توجه به شکل فوق، اوربیتال s کروی بوده و تنها به یک صورت میتواند در فضا قرار گیرد. اما مثلا اوربیتال p میتواند هم در راستای محور z و هم در راستای محور x جهتگیری کند. از این رو به عدد سومی تحت عنوان m یا عدد کوانتومی مغناطیسی نیازمندیم تا این جهتگیری اوربیتالها را نشان دهیم. بنابراین عدد m جهتگیری اوربیتال را در فضا نشان میدهد. عدد کوانتومی مغناطیسیِ یک اوربیتال، بین L- و L+ قرار دارد. برای نمونه اعداد کوانتومی مغناطیسی برای اوربیتال p که L مربوط با آن ۱ است، برابر با 1+,1,0- در نظر گرفته میشوند.
اگر الکترون را به صورت یک کره در نظر بگیریم، با استفاده از ۳ عدد معرفی شده در بالا میتواند جهت حرکت آن را در فضا مشخص کرد. اما این الکترون، به دور خودش نیز در حال چرخش است. این چرخش را با عدد کوانتومی اسپینی یا ms نشان میدهند. بنابراین یک الکترون میتواند تنها ساعتگرد (s=-1/2) و یا پادساعتگرد (s=+1/2) چرخش کند. در شکل زیر چرخش الکترون در این دو حالت نشان داده شده است.
همانطور که بیان شد هر اوربیتال دارای شکل مشخصی است که با توجه به اعداد کوانتومی معلوم میشوند. در ادامه اعداد کوانتومی مرتبط با هر اوبیتال و نحوه قرار گرفتن الکترونها در اوربیتالها را بیان خواهیم کرد.
در هر لایه یا به عبارتی در هر n، تعداد n-1 اوربیتال متفاوت میتواند قرار گیرد. برای نمونه در لایه اول تنها اوربیتال l=0 یا همان اوربیتال کروی وجود دارد. در n=2 دو اوربیتالِ کرویِ (l=0) و دمبلی (l=1) میتوانند قرار گیرند. از طرفی اوربیتال کروی تنها به یک شکل میتواند در فضا قرار گیرد، از این رو m آن تنها برابر با ۰ میتواند باشد. این در حالی است که اوربیتال دمبلی به ۳ شکل میتواند در فضا قرار گیرد، در نتیجه m=-1,0,+1 است. شکل زیر دو اوربیتال s و p را نشان میدهد.
به همین صورت اعداد هر اوربیتال معلوم میشوند. برای نمونه اوربیتال p (یا همان دمبلی) را در نظر بگیرید که در لایه سوم قرار گرفته است. برای این اوربیتال اعداد کوانتومی بهصورت زیر هستند.
توجه داشته باشید که عدد کوانتومی اسپینی برای یک الکترون تعریف میشود، به همین دلیل این عدد در بالا ارائه نشده. اوربیتالهای با l=1 (اوربیتال p) به بالا دارای شکلهایی بسیار پیچیده هستند که بهصورت گوناگونی میتوانند در فضا قرار گیرند. در جدول زیر ترتیب لایهها و زیرلایهها (اوربیتالها) برای چهار لایه اول ارائه شده است.
در جدول بالا ستونی تحت عنوان تعداد الکترونها وجود دارد. این ستون ظرفیت تعداد الکترونهای قرار گرفته در هر اوربیتال را نشان میدهد. برای نمونه اوربیتال p در سه جهت میتواند در فضا قرار گیرد. از طرفی در هرکدام از این حالات ۲ الکترون میتواند در اوربیتال مذکور وجود داشته باشد؛ بنابراین ظرفیت این اوربیتال برابر با ۶=۳×۲ است. البته ظرفیت هر اوربیتال با عدد L را میتوان با استفاده از فرمولِ $$2(2L+1)$$ نیز بدست آورد.
در تصویر زیر، شکل اوربیتالهای s,p,d,f نشان داده شده.
الکترونهای یک اتم با نظم مشخصی در اوربیتالها قرار میگیرند. در ابتدا لایههای با انرژی کمتر توسط الکترونها پر شده و پس از آن لایههای دورتر توسط آنها اشغال میشوند. با استفاده از «اصل آفبا» (Aufbau Principle) میتوان ترتیب الکترونها را در پر کردن اوربیتالها معلوم کرد.
در این اصل در ابتدا لایه با n کمتر توسط الکترونها اشغال میشوند. همچنین در یک لایه، ابتدا اوربیتال با انرژی کمتر پر میشود. برای نمونه در لایه دوم هر دو اوربیتالِ p و s وجود دارند. اما با توجه به انرژی کمتر اوربیتال s، در ابتدا این اوربیتال پر میشود. اما گاهی اوربیتال p در لایهای پایینتر به نسبت اوربیتال s قرار دارد. به نظر شما در این حالت اولویت با شماره لایه یا شکل اوربیتال است؟ در این حالت لایهای زودتر پر میشود که:
بر اساس دو الگوی بالا، الکترونها بهترتیب در اوربیتالهای زیر قرار میگیرند:
همانطور که در فرمول بالا میبینید در ابتدا شماره لایه و پس از آن حرف مربوط به زیرلایه (یا همان اوربیتال) نوشته میشود. البته بهمنظور به خاطر سپردنِ عبارت فوق میتوانید از تصویر زیر نیز استفاده کنید.
همانطور که در بالا نیز بیان شد، هر اوربیتال میتواند $$2(2L+1)$$ الکترون را در خود نگه دارد. برای نوشتن آرایش الکترونی یک اتم میتوان بهترتیب پر شدن، اوربیتالها را نوشت. در بالای هر اوربیتال ظرفیت مربوط به آن نوشته میشود. در ادامه آرایش الکترونی چندین اتم برای نمونه ارائه شدهاند. البته بعضی مواقع اوربیتالها را بهصورت مربع نشان میدهند. همچنین الکترونها را با فلشهایی نمایش میدهند که جهت آن، اسپین الکترون را نشان میدهد. جهت درک بهتر به مثالهای زیر توجه فرمایید. نمادهای استفاده شده در نوشتن آرایش الکترونی مطابق با الگوی زیر تعریف میشوند.
آرایش الکترونی اتم لیتیوم به چه صورت است؟
همانطور که احتمالا میدانید عدد اتمی لیتیوم، ۳ در نتیجه مجموع الکترونهای اشغال شده در اوربیتالهایش نیز برابر با ۳ است؛ مطابق با اصل آفبا، آرایش الکترونی اتم لیتیوم بهصورت زیر خواهد بود.
همانطور که میبینید در لایه اول اوربیتال s پر شده، اما در لایه دوم تنها یک الکترون در اوربیتال s قرار گرفته است. توجه داشته باشید که جهت بالا و پایین، جهت چرخش الکترون دور خودش -یا همان اسپین- را نشان میدهد.
آرایش الکترونی اتم کربن به چه شکل است؟
عدد اتمی کربن برابر با ۶ است. در نتیجه مجموع الکترونهای موجود در اوربیتالها بایستی برابر با ۶ باشد. توجه داشته باشید که در ابتدا یک اوربیتال بایستی پر شده و سپس اوربیتال بعدی را پر کنید. در زیر آرایش الکترونی اتم کربن رسم شده.
در آرایش بالا هر خانه نشان دهنده یک جهت از اوربیتال است. با توجه به اینکه اوربیتال p به ۳ شکل در فضا قرار میگیرد، بنابراین از سه خانه برای نشان دادن آن استفاده شده است. بهمنظور رسم فلشها، از چپ به راست در هر خانه یک فلش رو به بالا قرار داده و به همین شکل اوربیتال را پر کنید. مجموعِ کل فلشها بایستی برابر با عدد اتمی اتمِ مذکور باشد. پیشنهاد میکنیم چندین آرایش الکترونی را برای اتمهای مختلف نوشته و صحت آن با توجه به جدول زیر مورد بررسی قرار دهید.
البته با توجه به پایدار بودن عناصر نجیب، میتوان با استفاده از آنها نیز آرایش الکترونی را بیان کرد. برای نمونه در زیر آرایش الکترونی اتم کربن بر اساس آرایش هلیوم ارائه شده است.
توجه داشته باشید که به منظور نوشتن آرایش الکترونی یونها، عدد اتمی برابر با تعداد الکترونها نیست. برای نمونه در زیر آرایش الکترونی اتم آهن (Fe) و در نتیجه یونِ آهن (2+Fe) ارائه شده است.
در صورت علاقهمندی به مباحث مرتبط در زمینه فیزیک و شیمی، آموزشهای زیر نیز به شما پیشنهاد میشوند:
چگونه آرایش الکترونی بنویسیم
^^
مجید عوض زاده (+)
«مجید عوضزاده»، فارغ التحصیل مقطع کارشناسی ارشد رشته مهندسی مکانیک از دانشگاه تهران است. فیزیک، ریاضیات و مهندسی مکانیک از جمله مباحث مورد علاقه او هستند که در رابطه با آنها تولید محتوا میکند.
بر اساس رای 195 نفر
آیا این مطلب برای شما مفید بود؟
واقن فوق العاده درس دادین این مطلبو و کامل یادگرفتم
دستتون درد نکنه واقن مرسی بابت زحماتی ک میکشید .
دمتون گرم
سر کلاس استاد که چیزی نفهمیدم. اما اینجا همه چیز رو متوجه شدم عالی.
لینک مطلب رو برای دوستام هم فرستادم
دستتون درد نکنه
به نام خدا
با سلام و عرض ادب و احترام
برای شما از خداوند متعال آرزوی موفقیت روزافزون دارم. بسیار ممنون، زحمت کشیدید و مطالب مفیدی ارائه دادید.
واقعا درسی ک اقای بهنام محمدیان میدن بهترین و عالیترینه و کاملا بی نقصه و من کلا درسو یاد میگیرم
ب امید موفقیت های بیشتررررررر …ممنونم ازتون
خیلی عالی بود.
ممنونم
بعد از سال ها فاصله گرفتن از شیمی دبیرستان، این مطلب به خوبی، خیلی عالی، مطالب رو یادآوری کرد.
ممنون. خیلی خوب بود
خیلی عالی بود بعد از مدت ها یه تدریس خوب واسه این مبحث دیدم🌹
عالی ممنون واقعا خیلی خوب توضیح دادید. فقط اگه میشه توی اموزشاتتون ، انتهای هر اموزش فرمول ها و رابطه ها و مطالب خیلی مهم رو که توضیح داده شده رو یه جا مثلا توی جدول جمع کنین تا دسترسی بهش سریع تر و راحت تر بشه. مثل همون تقلب نامه هایی که منتشر میکنید. بازم ممنون با تشکر از سایت خوبتون.
با سلام. الان برای اوربیتال ۲p طبق شکل هسته در کجای شکل قرار میگیره؟ چون از اونجایی که الکترون به دور هسته می چرخه باید یه شکل کروی داشته باشه و یه مقدار شکل ها غیر عادیه.
مرسی خیلی به من کمک کرد.
خوب ولی کاش با فیلم توضیح میدادید .
بسیار عالی ممنونم
خیلی عالی کامل و بی نقص
تشکرمیکنم ازمجله فرادرس
نشانی ایمیل شما منتشر نخواهد شد. بخشهای موردنیاز علامتگذاری شدهاند *
سازمان علمی و آموزشی «فرادرس» (Faradars) از قدیمیترین وبسایتهای یادگیری آنلاین است که توانسته طی بیش از ده سال فعالیت خود بالغ بر ۱۲۰۰۰ ساعت آموزش ویدیویی در قالب فراتر از ۲۰۰۰ عنوان علمی، مهارتی و کاربردی را منتشر کند و به بزرگترین پلتفرم آموزشی ایران مبدل شود.
فرادرس با پایبندی به شعار «دانش در دسترس همه، همیشه و همه جا» با همکاری بیش از ۱۸۰۰ مدرس برجسته در زمینههای علمی گوناگون از جمله آمار و دادهکاوی، هوش مصنوعی، برنامهنویسی، طراحی و گرافیک کامپیوتری، آموزشهای دانشگاهی و تخصصی، آموزش نرمافزارهای گوناگون، دروس رسمی دبیرستان و پیش دانشگاهی، آموزشهای دانشآموزی و نوجوانان، آموزش زبانهای خارجی، مهندسی برق، الکترونیک و رباتیک، مهندسی کنترل، مهندسی مکانیک، مهندسی شیمی، مهندسی صنایع، مهندسی معماری و مهندسی عمران توانسته بستری را فراهم کند تا افراد با شرایط مختلف زمانی، مکانی و جسمانی بتوانند با بهرهگیری از آموزشهای با کیفیت، به روز و مهارتمحور همواره به یادگیری بپردازند. شما هم با پیوستن به جمع بزرگ و بالغ بر ۶۰۰ هزار نفری دانشجویان و دانشآموزان فرادرس و با بهرهگیری از آموزشهای آن، میتوانید تجربهای متفاوت از علم و مهارتآموزی داشته باشید.
مشاهده بیشتر
هر گونه بهرهگیری از مطالب مجله فرادرس به معنی پذیرش شرایط استفاده از آن بوده و کپی بخش یا کل هر کدام از مطالب، تنها با کسب مجوز مکتوب امکان پذیر است.
© فرادرس ۱۳۹۹
پیشتر در وبلاگ فرادرس مدل اتمی بور را توضیح دادیم. مدل اتمی بور مدلی یکبعدی است که تنها از یک عدد جهت توصیف الکترونهای یک اتم استفاده میکند. این عدد همان n است که نشان دهنده لایهای است که الکترون در آن میچرخد. همچنین مدل مذکور تنها میتواند ویژگیهای اتم هیدروژن را توجیه کند.
محتوای این مطلب جهت یادگیری بهتر و سریعتر آن، در انتهای متن به صورت ویدیویی نیز ارائه شده است.
«اروین شرودینگر» (Erwin Schrödinger)، در سال ۱۹۲۶ با استفاده از محاسبات پیچیده ریاضی نشان داد که الکترونهای یک اتم در مسیرهایی سهبعدی حرکت میکنند؛ از این رو به سه عدد جهت توصیف الکترونها نیازمندیم. البته به عدد چهارمی نیز بهمنظور نشان دادن نحوه حرکت الکترون به دور خودش نیازمند هستیم. هر الکترون در فضایی ابری تحت عنوان اوربیتال در حال حرکت است. نحوه این حرکت و آرایش الکترونها در شکلگیری پیوندهای شیمیایی بسیار تاثیرگذار هستند. با استفاده از اعداد کوانتومی که در ادامه به آنها خواهیم پرداخت، میتوان اوربیتالها را به شکلی دقیقتر توصیف کرد.
شرودینگر با حل معادلاتش سه عدد را جهت توصیف الکترونهای یک اتم ارائه داد. این اعداد عبارتند از:
عدد کوانتومی اصلی یا n، نشان دهنده اندازه و انرژی اوربیتال است. منظور از اندازه اوربیتال، فاصله الکترونها از هسته اتم است. هرچه اندازه این عدد بیشتر باشد، اندازه و انرژی اوربیتال نیز بزرگتر خواهد بود. تمامی الکترونهایی که n آنها با هم برابر است، در فاصلهای یکسان از هسته اتم قرار میگیرند.
چگونه آرایش الکترونی بنویسیم
L یا عدد کوانتومی فرعی، نشاندهنده شکل اوربیتال است. یک لایه با عدد کوانتومی n میتواند از n-1 اوربیتال مختلف تشکیل شده باشد. شکلهای یک اوربیتال را با نمادهای $$s,p,d,f,…$$ نشان میدهند. برای نمونه L=۰ نشان دهنده اوربیتال s یا L=۱ اوربیتال p را نشان میدهد. تصویر ارائه شده، شکل اوربیتالهای مختلف را نمایش میدهد.
با توجه به شکل فوق، اوربیتال s کروی بوده و تنها به یک صورت میتواند در فضا قرار گیرد. اما مثلا اوربیتال p میتواند هم در راستای محور z و هم در راستای محور x جهتگیری کند. از این رو به عدد سومی تحت عنوان m یا عدد کوانتومی مغناطیسی نیازمندیم تا این جهتگیری اوربیتالها را نشان دهیم. بنابراین عدد m جهتگیری اوربیتال را در فضا نشان میدهد. عدد کوانتومی مغناطیسیِ یک اوربیتال، بین L- و L+ قرار دارد. برای نمونه اعداد کوانتومی مغناطیسی برای اوربیتال p که L مربوط با آن ۱ است، برابر با 1+,1,0- در نظر گرفته میشوند.
اگر الکترون را به صورت یک کره در نظر بگیریم، با استفاده از ۳ عدد معرفی شده در بالا میتواند جهت حرکت آن را در فضا مشخص کرد. اما این الکترون، به دور خودش نیز در حال چرخش است. این چرخش را با عدد کوانتومی اسپینی یا ms نشان میدهند. بنابراین یک الکترون میتواند تنها ساعتگرد (s=-1/2) و یا پادساعتگرد (s=+1/2) چرخش کند. در شکل زیر چرخش الکترون در این دو حالت نشان داده شده است.
همانطور که بیان شد هر اوربیتال دارای شکل مشخصی است که با توجه به اعداد کوانتومی معلوم میشوند. در ادامه اعداد کوانتومی مرتبط با هر اوبیتال و نحوه قرار گرفتن الکترونها در اوربیتالها را بیان خواهیم کرد.
در هر لایه یا به عبارتی در هر n، تعداد n-1 اوربیتال متفاوت میتواند قرار گیرد. برای نمونه در لایه اول تنها اوربیتال l=0 یا همان اوربیتال کروی وجود دارد. در n=2 دو اوربیتالِ کرویِ (l=0) و دمبلی (l=1) میتوانند قرار گیرند. از طرفی اوربیتال کروی تنها به یک شکل میتواند در فضا قرار گیرد، از این رو m آن تنها برابر با ۰ میتواند باشد. این در حالی است که اوربیتال دمبلی به ۳ شکل میتواند در فضا قرار گیرد، در نتیجه m=-1,0,+1 است. شکل زیر دو اوربیتال s و p را نشان میدهد.
به همین صورت اعداد هر اوربیتال معلوم میشوند. برای نمونه اوربیتال p (یا همان دمبلی) را در نظر بگیرید که در لایه سوم قرار گرفته است. برای این اوربیتال اعداد کوانتومی بهصورت زیر هستند.
توجه داشته باشید که عدد کوانتومی اسپینی برای یک الکترون تعریف میشود، به همین دلیل این عدد در بالا ارائه نشده. اوربیتالهای با l=1 (اوربیتال p) به بالا دارای شکلهایی بسیار پیچیده هستند که بهصورت گوناگونی میتوانند در فضا قرار گیرند. در جدول زیر ترتیب لایهها و زیرلایهها (اوربیتالها) برای چهار لایه اول ارائه شده است.
در جدول بالا ستونی تحت عنوان تعداد الکترونها وجود دارد. این ستون ظرفیت تعداد الکترونهای قرار گرفته در هر اوربیتال را نشان میدهد. برای نمونه اوربیتال p در سه جهت میتواند در فضا قرار گیرد. از طرفی در هرکدام از این حالات ۲ الکترون میتواند در اوربیتال مذکور وجود داشته باشد؛ بنابراین ظرفیت این اوربیتال برابر با ۶=۳×۲ است. البته ظرفیت هر اوربیتال با عدد L را میتوان با استفاده از فرمولِ $$2(2L+1)$$ نیز بدست آورد.
در تصویر زیر، شکل اوربیتالهای s,p,d,f نشان داده شده.
الکترونهای یک اتم با نظم مشخصی در اوربیتالها قرار میگیرند. در ابتدا لایههای با انرژی کمتر توسط الکترونها پر شده و پس از آن لایههای دورتر توسط آنها اشغال میشوند. با استفاده از «اصل آفبا» (Aufbau Principle) میتوان ترتیب الکترونها را در پر کردن اوربیتالها معلوم کرد.
در این اصل در ابتدا لایه با n کمتر توسط الکترونها اشغال میشوند. همچنین در یک لایه، ابتدا اوربیتال با انرژی کمتر پر میشود. برای نمونه در لایه دوم هر دو اوربیتالِ p و s وجود دارند. اما با توجه به انرژی کمتر اوربیتال s، در ابتدا این اوربیتال پر میشود. اما گاهی اوربیتال p در لایهای پایینتر به نسبت اوربیتال s قرار دارد. به نظر شما در این حالت اولویت با شماره لایه یا شکل اوربیتال است؟ در این حالت لایهای زودتر پر میشود که:
بر اساس دو الگوی بالا، الکترونها بهترتیب در اوربیتالهای زیر قرار میگیرند:
همانطور که در فرمول بالا میبینید در ابتدا شماره لایه و پس از آن حرف مربوط به زیرلایه (یا همان اوربیتال) نوشته میشود. البته بهمنظور به خاطر سپردنِ عبارت فوق میتوانید از تصویر زیر نیز استفاده کنید.
همانطور که در بالا نیز بیان شد، هر اوربیتال میتواند $$2(2L+1)$$ الکترون را در خود نگه دارد. برای نوشتن آرایش الکترونی یک اتم میتوان بهترتیب پر شدن، اوربیتالها را نوشت. در بالای هر اوربیتال ظرفیت مربوط به آن نوشته میشود. در ادامه آرایش الکترونی چندین اتم برای نمونه ارائه شدهاند. البته بعضی مواقع اوربیتالها را بهصورت مربع نشان میدهند. همچنین الکترونها را با فلشهایی نمایش میدهند که جهت آن، اسپین الکترون را نشان میدهد. جهت درک بهتر به مثالهای زیر توجه فرمایید. نمادهای استفاده شده در نوشتن آرایش الکترونی مطابق با الگوی زیر تعریف میشوند.
آرایش الکترونی اتم لیتیوم به چه صورت است؟
همانطور که احتمالا میدانید عدد اتمی لیتیوم، ۳ در نتیجه مجموع الکترونهای اشغال شده در اوربیتالهایش نیز برابر با ۳ است؛ مطابق با اصل آفبا، آرایش الکترونی اتم لیتیوم بهصورت زیر خواهد بود.
همانطور که میبینید در لایه اول اوربیتال s پر شده، اما در لایه دوم تنها یک الکترون در اوربیتال s قرار گرفته است. توجه داشته باشید که جهت بالا و پایین، جهت چرخش الکترون دور خودش -یا همان اسپین- را نشان میدهد.
آرایش الکترونی اتم کربن به چه شکل است؟
عدد اتمی کربن برابر با ۶ است. در نتیجه مجموع الکترونهای موجود در اوربیتالها بایستی برابر با ۶ باشد. توجه داشته باشید که در ابتدا یک اوربیتال بایستی پر شده و سپس اوربیتال بعدی را پر کنید. در زیر آرایش الکترونی اتم کربن رسم شده.
در آرایش بالا هر خانه نشان دهنده یک جهت از اوربیتال است. با توجه به اینکه اوربیتال p به ۳ شکل در فضا قرار میگیرد، بنابراین از سه خانه برای نشان دادن آن استفاده شده است. بهمنظور رسم فلشها، از چپ به راست در هر خانه یک فلش رو به بالا قرار داده و به همین شکل اوربیتال را پر کنید. مجموعِ کل فلشها بایستی برابر با عدد اتمی اتمِ مذکور باشد. پیشنهاد میکنیم چندین آرایش الکترونی را برای اتمهای مختلف نوشته و صحت آن با توجه به جدول زیر مورد بررسی قرار دهید.
البته با توجه به پایدار بودن عناصر نجیب، میتوان با استفاده از آنها نیز آرایش الکترونی را بیان کرد. برای نمونه در زیر آرایش الکترونی اتم کربن بر اساس آرایش هلیوم ارائه شده است.
توجه داشته باشید که به منظور نوشتن آرایش الکترونی یونها، عدد اتمی برابر با تعداد الکترونها نیست. برای نمونه در زیر آرایش الکترونی اتم آهن (Fe) و در نتیجه یونِ آهن (2+Fe) ارائه شده است.
در صورت علاقهمندی به مباحث مرتبط در زمینه فیزیک و شیمی، آموزشهای زیر نیز به شما پیشنهاد میشوند:
چگونه آرایش الکترونی بنویسیم
^^
مجید عوض زاده (+)
«مجید عوضزاده»، فارغ التحصیل مقطع کارشناسی ارشد رشته مهندسی مکانیک از دانشگاه تهران است. فیزیک، ریاضیات و مهندسی مکانیک از جمله مباحث مورد علاقه او هستند که در رابطه با آنها تولید محتوا میکند.
بر اساس رای 195 نفر
آیا این مطلب برای شما مفید بود؟
واقن فوق العاده درس دادین این مطلبو و کامل یادگرفتم
دستتون درد نکنه واقن مرسی بابت زحماتی ک میکشید .
دمتون گرم
سر کلاس استاد که چیزی نفهمیدم. اما اینجا همه چیز رو متوجه شدم عالی.
لینک مطلب رو برای دوستام هم فرستادم
دستتون درد نکنه
به نام خدا
با سلام و عرض ادب و احترام
برای شما از خداوند متعال آرزوی موفقیت روزافزون دارم. بسیار ممنون، زحمت کشیدید و مطالب مفیدی ارائه دادید.
واقعا درسی ک اقای بهنام محمدیان میدن بهترین و عالیترینه و کاملا بی نقصه و من کلا درسو یاد میگیرم
ب امید موفقیت های بیشتررررررر …ممنونم ازتون
خیلی عالی بود.
ممنونم
بعد از سال ها فاصله گرفتن از شیمی دبیرستان، این مطلب به خوبی، خیلی عالی، مطالب رو یادآوری کرد.
ممنون. خیلی خوب بود
خیلی عالی بود بعد از مدت ها یه تدریس خوب واسه این مبحث دیدم🌹
عالی ممنون واقعا خیلی خوب توضیح دادید. فقط اگه میشه توی اموزشاتتون ، انتهای هر اموزش فرمول ها و رابطه ها و مطالب خیلی مهم رو که توضیح داده شده رو یه جا مثلا توی جدول جمع کنین تا دسترسی بهش سریع تر و راحت تر بشه. مثل همون تقلب نامه هایی که منتشر میکنید. بازم ممنون با تشکر از سایت خوبتون.
با سلام. الان برای اوربیتال ۲p طبق شکل هسته در کجای شکل قرار میگیره؟ چون از اونجایی که الکترون به دور هسته می چرخه باید یه شکل کروی داشته باشه و یه مقدار شکل ها غیر عادیه.
مرسی خیلی به من کمک کرد.
خوب ولی کاش با فیلم توضیح میدادید .
بسیار عالی ممنونم
خیلی عالی کامل و بی نقص
تشکرمیکنم ازمجله فرادرس
نشانی ایمیل شما منتشر نخواهد شد. بخشهای موردنیاز علامتگذاری شدهاند *
سازمان علمی و آموزشی «فرادرس» (Faradars) از قدیمیترین وبسایتهای یادگیری آنلاین است که توانسته طی بیش از ده سال فعالیت خود بالغ بر ۱۲۰۰۰ ساعت آموزش ویدیویی در قالب فراتر از ۲۰۰۰ عنوان علمی، مهارتی و کاربردی را منتشر کند و به بزرگترین پلتفرم آموزشی ایران مبدل شود.
فرادرس با پایبندی به شعار «دانش در دسترس همه، همیشه و همه جا» با همکاری بیش از ۱۸۰۰ مدرس برجسته در زمینههای علمی گوناگون از جمله آمار و دادهکاوی، هوش مصنوعی، برنامهنویسی، طراحی و گرافیک کامپیوتری، آموزشهای دانشگاهی و تخصصی، آموزش نرمافزارهای گوناگون، دروس رسمی دبیرستان و پیش دانشگاهی، آموزشهای دانشآموزی و نوجوانان، آموزش زبانهای خارجی، مهندسی برق، الکترونیک و رباتیک، مهندسی کنترل، مهندسی مکانیک، مهندسی شیمی، مهندسی صنایع، مهندسی معماری و مهندسی عمران توانسته بستری را فراهم کند تا افراد با شرایط مختلف زمانی، مکانی و جسمانی بتوانند با بهرهگیری از آموزشهای با کیفیت، به روز و مهارتمحور همواره به یادگیری بپردازند. شما هم با پیوستن به جمع بزرگ و بالغ بر ۶۰۰ هزار نفری دانشجویان و دانشآموزان فرادرس و با بهرهگیری از آموزشهای آن، میتوانید تجربهای متفاوت از علم و مهارتآموزی داشته باشید.
مشاهده بیشتر
هر گونه بهرهگیری از مطالب مجله فرادرس به معنی پذیرش شرایط استفاده از آن بوده و کپی بخش یا کل هر کدام از مطالب، تنها با کسب مجوز مکتوب امکان پذیر است.
© فرادرس ۱۳۹۹
%PDF-1.5
%
58 0 obj>
endobj
xref
58 33
0000000016 00000 n
0000001458 00000 n
0000000956 00000 n
0000001754 00000 n
0000001797 00000 n
0000001952 00000 n
0000002248 00000 n
0000002297 00000 n
0000002484 00000 n
0000010778 00000 n
0000011504 00000 n
0000012039 00000 n
0000012749 00000 n
0000013389 00000 n
0000014440 00000 n
0000014611 00000 n
0000015258 00000 n
0000015881 00000 n
0000016551 00000 n
0000017570 00000 n
0000018614 00000 n
0000018776 00000 n
0000018930 00000 n
0000019643 00000 n
0000020253 00000 n
0000020570 00000 n
0000021167 00000 n
0000021189 00000 n
0000023837 00000 n
0000023871 00000 n
0000023909 00000 n
0000035913 00000 n
0000035966 00000 n
trailer
]>>
startxref
0
%%EOF
60 0 obj>stream
xb“`b“yAbl,& w6L_Y`ЫaկSQܢ˛Yl{ K|>Ϣc”,4VX(f]cR;Dﵩ_t[%TI,-l(onSBLƂ]m”/w,63Y”=lW!XcxD”|aSP
[D_$lZ”.9M!&@lla